Chimie analytique-Moeung Sotheara
1. គេមានសូលុយស្យុងមួយដែលមានផ្ទុកសារធាតុ x ។ ចូរជ្រើសរើសចម្លើយដែលត្រឹមត្រូវ :
���. Chimie analytique qualitative អាចអោយយើងដឹងថាសារធាតុ x ជាប៉ារ៉ាសេតាម៉ុល ។
���. Chimie analytique qualitative អាចអោយយើងដឹងថាសារធាតុ x មានកំហាប់ 0.1 M ។
���. Chimie analytique quantitative អាចអោយយើងដឹងថាសារធាតុ x ជាប៉ារ៉ាសេតាម៉ុល ។
���. ចម្លើយ ខ និង គ ។
2. គេមានសូលុយស្យុងមួយដែលមានផ្ទុកសារធាតុ x ។ ចូរជ្រើសរើសចម្លើយដែលត្រឹមត្រូវ :
���. Chimie analytique quantitative អាចអោយយើងដឹងថាសារធាតុ x ជាប៉ារ៉ាសេតាម៉ុល ។
ខ. Chimie analytique quantitative អាចអោយយើងដឹងថាសារធាតុ x មានកំហាប់ 0.1 M ។
���. Chimie analytique qualitative អាចអោយយើងដឹងថាសារធាតុ x មានកំហាប់ 0.1 M ។
���. ចម្លើយ ក និង គ ។
3. ខាងក្រោមនេះណាមួយជាទំនាក់ទំនងរវាង pH និង pKa របស់អាស៊ីតខ្សោយ :
���. pH = pKa – log [A^- ]/[HA]
���. pH = pKa + log
���. pH = pKa + log [HA]/[A^- ]
���. pH = 〖10〗^(-pKa)
4. ខាងក្រោមណាមួយជាសូលុយស្យុង tampon :
ក. ល្បាយសូលុយស្យុង អាស៊ីតអាសេទិច (CH3COOH) និង អេតាណូអាត (CH3COO-)
���. សូលុយស្យុង ប្រាក់នីត្រាត (AgNO3)
���. សូលុយស្យុងអាស៊ីតក្លរីឌ្រិច (HCl)
���. ល្បាយសូលុយស្យុង អាស៊ីតអាសេទិច (CH3COOH) និង មេតាណូអាត (HCOO-)
5. ខាងក្រោមណាមួយជាសមីការនៃការបំបែករបស់អាស៊ីតអាសេទិចក្នុងទឹក :
���. CH3COOH + H2O CH3COO- + H3O+
���. CH3COOH + H2O ⇌ CH3COO- + H3O+
���. HCOOH + H2O ⇌ HCOO- + H3O+
���. HCOO- + H2O ⇌ HCOOH + OH-
6. គូអាស៊ីត-បាសមួយមាន pKa=4 ចូរជ្រើសរើសចម្លើយដែលត្រឹមត្រូវ :
���. Ka = 〖10〗^(-4)
���. Ka = -log4
���. Kb = 〖10〗^(-10)
���. ចម្លើយ ក និង គ
7. អាស៊ីត A មាន pKa = 3.5 អាស៊ីត B មាន pKa = 4.5 ។ ចូរជ្រើសរើសចម្លើយដែលត្រឺមត្រូវ :
���. អាស៊ីត A មានកំលាំងអាស៊ីតខ្លាំងជាង អាស៊ីត B
���. អាស៊ីត B មានកំលាំងអាស៊ីតខ្លាំងជាង អាស៊ីត A
���. អាស៊ីត A មានកំលាំងអាស៊ីតខ្សោយជាង អាស៊ីត B
���. អាស៊ីតទាំងពីរមានកំលាំងអាស៊ីតស្មើគ្នា
8. ចូរជ្រើសរើសចម្លើយដែលត្រឺមត្រូវ។ នៅក្នុងល្បាយសូលុយស្យុងមួយគេមានកំហាប់អាស៊ីតអាសេទិច 0.1 M និង អេតាណូអាត 0.1 M។ ដោយដឹងថា pKa នៃ គូ អាស៊ីតអាសេទិច/អេតាណូអាត = 4.7។ pH នៃល្បាយសូលុយស្យុងនេះគឺ :
���. pH = 4.7
���. pH = 5.7
���. pH = 6.5
���. pH = 3.5
9. ចូរជ្រើសរើសចម្លើយដែលត្រឺមត្រូវ។ នៅក្នុងល្បាយសូលុយស្យុងមួយគេមានកំហាប់អាស៊ីតអាសេទិច 0.1 M និង អេតាណូអាត 0.2 M។ ដោយដឹងថា pKa នៃ គូ អាស៊ីតអាសេទិច/អេតាណូអាត = 4.7។ pH នៃល្បាយសូលុយស្យុងនេះគឺ :
���. pH = 5.0
���. pH = 4.7
���. pH = 4.4
���. pH = 3.5
10. ចូរជ្រើសរើសចម្លើយដែលត្រឺមត្រូវ។ នៅក្នុងល្បាយសូលុយស្យុងមួយគេមានកំហាប់អាស៊ីតអាសេទិច 0.2 M និង អេតាណូអាត 0.1 M។ ដោយដឹងថា pKa នៃ គូ អាស៊ីតអាសេទិច/អេតាណូអាត = 4.7។ pH នៃល្បាយសូលុយស្យុងនេះគឺ :
ក. pH = 5.0
���. pH = 4.7
���. pH = 4.4
ឃ. pH = 3.5
11. គេមានសូលុយស្យុងដែលមានផ្ទុកគូអាស៊ីត-បាស HA/A- ដែលមាន pKa = 4,2។ បើសូលុយស្យុងនេះមាន pH = 1 ចូរជ្រើសរើសចម្លើយដែលត្រឹមត្រូវ :
���. ([A^-])/([HA]) = 〖10〗^(-3.2)
���. ([A^-])/( [HA]) = 〖10〗^(-5.2)
���. ([A^-])/([HA]) = 〖10〗^(-4.2)
���. ([A^-])/([HA]) = 〖10〗^(-5.0)
12. គេមានសូលុយស្យុងដែលមានផ្ទុកគូអាស៊ីត-បាស HA/A- ដែលមាន pKa = 4,2។ បើសូលុយស្យុងនេះមាន pH = 10 ចូរជ្រើសរើសចម្លើយដែលត្រឹមត្រូវ :
���. ([A^-])/([HA]) = 〖10〗^5.8
���.([A^-])/( [HA]) = 〖10〗^(-5.8)
���. ([A^-])/([HA]) = 〖10〗^4.2
���. ([A^-])/([HA]) = 〖10〗^(-5.0)
13. ចូរជ្រើសរើសចម្លើយត្រឹមត្រូវ។ សារធាតុ A មានម៉ាសម៉ូល 18 g/mol ។ សូលុយស្យុងនៃ A ដែលមានកំហាប់ 9% មាន molarité :
���. 0.09 M
���. 0.5 M
���. 5 M
���. 0.05 M
14.ខាងក្រោមនេះណាមួយមិនមែនជាលក្ខណ:របស់សូលុយស្យុង tampon :
���.pH របស់សូលុយស្យុង tampon មិនប្រែប្រួលដោយសារការពង្រាវទេ
���.pH របស់សូលុយស្យុង tampon ប្រែប្រួលតិចតួចពេលគេបន្ថែម H3O+
���.pH របស់សូលុយស្យុង tampon ប្រែប្រួលតិចតួចពេលគេបន្ថែម OH-
���.សូលុយស្យុង tampon ប្រែពណ៌ពេលគេបន្ថែមអាស៊ីតក្លរីឌ្រិច(HCl)
15. ចូរជ្រើសរើសចម្លើយត្រឹមត្រូវ។សូលុយស្យុងដែលផ្ទុក KNO3 50.5g (ម៉ាស់ម៉ូល=101 g/mol) មាន pH ស្មើនឹង :
ក. 0.3
���. 7
���. 0.5
ឃ. 2
16. ម៉ាស់ម៉ូលអាស៊ីតស៊ុលហ្វួរិច (H2SO4) ស្មើ 98g/mole ។ តើគេត្រូរំលាយអាស៊ីតស៊ុលហ្វួរិច ប៉ុន្មានក្រាមក្នុងទឹក 500 mL ដើម្បីទទួលបានសូលុយស្យុងដែលមាន pH= 2។ ចូរជ្រើសរើសចម្លើយត្រឹមត្រូវ :
���. 0.245 g
���. 0.530g
���. 98g
���. 0.980g
17. ម៉ាស់ម៉ូលអាស៊ីតក្លរីឌ្រិច (HCl) ស្មើ 36.5g/mole ។ តើគេត្រូរំលាយអាស៊ីតក្លរីឌ្រិច ប៉ុន្មានក្រាមក្នុងទឹក 500 mL ដើម្បីទទួលបានសូលុយស្យុងដែលមាន pH= 1។ ចូរជ្រើសរើសចម្លើយត្រឹមត្រូវ :
���. 1.825 g
���. 0.182g
គ. 36.5g
���. 0.365g
18.គេចង់កំណត់រកកំហាប់សារធាតុ A តាមវីធីសាស្រ្ត étalonnage (dosage par étalonnage)។ ដើម្បីអោយគេអាចប្រើវីធីសាស្រ្តនេះសំរាប់រកកំហាប់សារធាតុ A បាន វីធីសាស្រ្តនេះត្រូវបំពេញលក្ខខណ្ឌមួយចំនួនជាមុនសិន។ បើគេរៀបចំសូលុយស្យុង A ដែលមាន ៥ កំហាប់ផ្សេងគ្នា C1= 0.1 M, C2= 0.3 M, C3= 0.5 M, C4=0.9 M, C5=1.2 M, C6=1.5 M បន្ទាប់មកគេវាស់លក្ខណ:រូបនៅកំហាប់និមួយៗ។ គេទទួលបានក្រាបដូចខាងក្រោម តើលក្ខខណ្ឌណាមួយដែលត្រូវបានបំពេញ?
���. linéarité
���. spécificité
���. justesse
���. sensibilité
19.គេចង់កំណត់រកកំហាប់សារធាតុ A តាមវីធីសាស្រ្ត étalonnage (dosage par étalonnage)។ ដើម្បីអោយគេអាចប្រើវីធីសាស្រ្តនេះសំរាប់រកកំហាប់សារធាតុ A បាន វីធីសាស្រ្តនេះត្រូវបំពេញលក្ខខណ្ឌមួយចំនួនជាមុនសិន។ បើគេរៀបចំសូលុយស្យុង A ចំនួន 2 ដែលមានកំហាប់ក្បែរគ្នា C1=0.2 μg/mL និង C2=0.4 μg/mL។ ការធ្វើ dosage par étalonnage ផ្តល់តំលៃកំហាប់ C1=0.17 μg/mL និង C2=0.42 μg/mL។ តើលក្ខខណ្ឌណាមួយដែលត្រូវបានបំពេញ?
���. linéarité
���. spécificité
���. justesse
���. sensibilité
20.គេចង់កំណត់រកកំហាប់សារធាតុ A តាមវីធីសាស្រ្ត étalonnage (dosage par étalonnage)។ ដើម្បីអោយគេអាចប្រើវីធីសាស្រ្តនេះសំរាប់រកកំហាប់សារធាតុ A បាន វីធីសាស្រ្តនេះត្រូវបំពេញលក្ខខណ្ឌមួយចំនួនជាមុនសិន។ បើគេរៀបចំសូលុយស្យុង A ដែលមានកំហាប់ C=0.8 μg/mL។ គេវាស់កំហាប់ ៣ ដង ដោយធ្វើ dosage par étalonnage។ តំលៃកំហាប់ដែលទទួលបានគឺ 0.75 , 0.78 និង 0.81 μg/mL។ តើលក្ខខណ្ឌណាមួយដែលត្រូវបានបំពេញ?
���. linéarité
���. spécificité
គ. justesse
���. sensibilité
21.គេចង់កំណត់រកកំហាប់សារធាតុ A តាមវីធីសាស្រ្ត étalonnage (dosage par étalonnage)។ ដើម្បីអោយគេអាចប្រើវីធីសាស្រ្តនេះសំរាប់រកកំហាប់សារធាតុ A បាន វីធីសាស្រ្តនេះត្រូវបំពេញលក្ខខណ្ឌមួយចំនួនជាមុនសិន។ បើគេរៀបចំសូលុយស្យុង A ដែលមានកំហាប់ C=0.8 μg/mL។ គេវាស់កំហាប់ដោយធ្វើ dosage par étalonnage។ តំលៃកំហាប់ដែលទទួលបានគឺ 0.77 μg/mL។ គេប្តូរលក្ខណមួយចំនួនក្នុងមន្ទីរពិសោធ(ដូចជាសីតុណ្ហភាព សំពាធបរិយាកាស …) អោយខុសពីមុនបន្តិច គេវាស់កំហាប់សូលុយស្យុង A ម្តងទៀត តំលៃកំហាប់ដែលទទួលបានគឺ 0.81 μg/mL។ តើលក្ខខណ្ឌណាមួយដែលត្រូវបានបំពេញ?
���. linéarité
���. spécificité
���. robustesse
���. sensibilité
22.គេចង់កំណត់រកកំហាប់សារធាតុ A តាមវីធីសាស្រ្ត étalonnage (dosage par étalonnage)។ ដើម្បីអោយគេអាចប្រើវីធីសាស្រ្តនេះសំរាប់រកកំហាប់សារធាតុ A បាន វីធីសាស្រ្តនេះត្រូវបំពេញលក្ខខណ្ឌមួយចំនួនជាមុនសិន។ បើសូលុយស្យុង A ត្រូវបានវាស់កំហាប់ 3 ដងដោយមនុស្សម្នាក់ក្នុងមន្ទីរពិសោធតែមួយ ដោយធ្វើ dosage par étalonnage។ តំលៃកំហាប់ដែលទទួលបានគឺ 0.5 , 0.51 និង 0.48 μg/mL។ តើលក្ខខណ្ឌណាមួយដែលត្រូវបានបំពេញ?
���. linéarité
���. spécificité
គ. répétabilité
���. sensibilité
23.គេចង់កំណត់រកកំហាប់សារធាតុ A តាមវីធីសាស្រ្ត étalonnage (dosage par étalonnage)។ ដើម្បីអោយគេអាចប្រើវីធីសាស្រ្តនេះសំរាប់រកកំហាប់សារធាតុ A បាន វីធីសាស្រ្តនេះត្រូវបំពេញលក្ខខណ្ឌមួយចំនួនជាមុនសិន។ បើសូលុយស្យុង A ត្រូវបានវាស់កំហាប់ 3 ដងដោយមនុស្ស 3នាក់ក្នុងមន្ទីរពិសោធតែមួយ ដោយធ្វើ dosage par étalonnage។ តំលៃកំហាប់ដែលទទួលបានគឺអ្នកទីមួយរកឃើញតំលៃកំហាប់ 0.48μg/mL អ្នកទីពីរឃើញ 0.51μg/mL និងអ្នកទីបីឃើញ 0.50 μg/mL។ តើលក្ខខណ្ឌណាមួយដែលត្រូវបានបំពេញ?
���. linéarité
���. spécificité
���. fidélité intermédiaire
���. sensibilité
25. ខាងក្រោមនេះ ណាមួយជាលក្ខណ:របស់សូលុយស្យុង tampon :
ក. pH របស់សូលុយស្យុង tampon មិនប្រែប្រួលដោយការពង្រាវសូលុយស្យុងទេ
���. pH របស់សូលុយស្យុង tampon ប្រែប្រួលតិចតួចពេលយើងបន្ថែមអ៊ីយ៉ុង H3O+
���. pH របស់សូលុយស្យុង tampon ប្រែប្រួលតិចតួចពេលយើងបន្ថែមអ៊ីយ៉ុង OH-
D. ឃ. ចម្លើយ ក ខ និង គ
26. គូរេដុក Cu2+/Cu មាន potentiel rédox Eo = 0.34 V ។ តើក្នុងចំណោមគូរេដុកខាងក្រោម ណាមួយដែលផ្តល់ រេដុកករ អោយមានប្រតិកម្មជាមួយ អ៊ីយ៉ុង Cu2+ ។
���. Al3+/Al ដែលមាន Eo= -1,66 V
���. MnO2/Mn2+ ដែលមាន Eo=1,23 V
���. Ag+/Ag ដែលមាន Eo=0,80 V
���. PbO2/Pb2+ ដែលមាន Eo=1,45 V
���.គ្មានចម្លើយត្រឹមត្រូវ
27. ខាងក្រោមនេះ ណាមួយជាចំនួនអុកស៊ីតកម្មរបស់ Mn នៅក្នុង MnO4-
���. +7
���. +4
���. -7
���. +2
28. ខាងក្រោមនេះ ណាមួយជាចំនួនអុកស៊ីតកម្មរបស់ Cr នៅក្នុង Cr2O72-
���. +6
���. +4
���. -7
���. +3
29. ក្នុងចំណោមឃ្លាខាងក្រោមនេះ ណាមួយដែលត្រឹមត្រូវ
���. ក្នុងពេលប្រតិកម្មអុកស៊ីតកម្ម ចំនួនអុកស៊ីតកម្មកើនឡើង
���. ក្នុងពេលប្រតិកម្មរេដុកកម្ម ចំនួនអុកស៊ីតកម្មមិនប្រែប្រួល
���. ក្នុងពេលប្រតិកម្មអុកស៊ីតកម្ម ចំនួនអុកស៊ីតកម្មមិនប្រែប្រួល
���.ក្នុងពេលប្រតិកម្មរេដុកកម្ម ចំនួនអុកស៊ីតកម្មកើនឡើង
30. ចូរជ្រើសរើសចម្លើយដែលត្រឹមត្រូវ។ខ្សែកោងខាងលើតំណាងអោយ :
���. Dosage អាស៊ីតដោយ បាស
���. Dosage បាសដោយ អាស៊ីត
���. Dosage រេដុកករ ដោយ អុកស៊ីតករ
���. Dosage អុកស៊ីតករ ដោយ រេដុកករ
31. សូលុយស្យុង titrante ណាមួយដែលគេប្រើជាទូទៅដើម្បី doser l’iode?
���. S2O32-
���. S4O62-
���. MnO4-
���. Cr2O72-
32. គេចាក់សូលុយស្យុង KI អោយលើសចូលទៅក្នុង សូលុយស្យុង hypochorite de sodium (NaClO) : ClO- + 2 I- + 2 H+ Cl- + I2 +H2O ។ L’iode ដែលកកើតត្រូវបាន dosé ដោយសូលុយស្យុង Thiosulfate de Na (Na2S2O3) : 2 S2O32- + I2 2 I- + S4O62- ប្រសិនគេដឹងថាគេប្រើ S2O32- អស់ 0,2 moles ។ ចូររកចំនួនម៉ូល NaClO ។
���. 0,2 moles
���. 0.4 moles
���. 0.1 moles
���. 0.05 moles
33. ខាងក្រោមនេះ ណាមួយជា réactif titrant réducteur ?
���. Solution de Fe2+
���. Solution thiosulfate de Na
���. Solution d’iode
���. ក និង ខ
34. ខាងក្រោមនេះ ណាមួយដែលត្រឹមត្រូវទាក់ទងនឹង manganimétrie ?
ក. មិនត្រូវការ indicateur coloré ទេ
���. Dosage ត្រូវធ្វើក្នុង មជ្ឈដ្ឋានអាស៊ីត
គ. ដោយសារ តម្លៃ Eo របស់គូរ MnO4-/Mn2+ ដែលធ្វើអោយ MnO4- មានកម្លាំង អុកស៊ីតករខ្លាំង
���. ក ខ និង គ
35. គេចង់ doser សារធាតុ X ដោយ Chromimétrie ។ គេចាក់សូលុយស្យុង Cr2O72- អោយលើសចូលទៅក្នុង សូលុយស្យុង X : X + Cr2O72- + 14 H+ 2 Cr3+ + 7 H2O + Y ។ បរិមាណ Cr2O72- ដែលលើសគេដាក់អោយមានប្រតិកម្មជាមួយ KI : Cr2O72- + 6 I- + 14H+ 2 Cr3+ + 7 H2O + 3 I2 ។ បន្ទាប់មក I2 ដែលកកើតត្រូវបានដាក់អោយមានប្រតិកម្មជាមួយ S2O32- : 2 S2O32- + I2 2 I- + S4O62- ។ បើគេដឹងថា ចំនួនម៉ូល Cr2O72- សរុបទាំងអស់ 0,5 moles ហើយ ចំនួនម៉ូល S2O32- ដែលគេប្រើស្មើនឹង 1,2 moles។ គណនាចំនួនម៉ូល X .
ក. 0,3 moles
���. ០,2 moles
���. ០,5 moles
���. 1,2 moles
36. លក្ខណ:មួយណាខាងក្រោមដែលទាក់ទងនឹង Iodométrie
���. Iode អាចជា indicateur coloré ខ្លួនឯង
���. មិនត្រូវការមជ្ឈដ្ឋានអាស៊ីត
���. យើងអាចប្រើ Iode ជាសូលុយស្យុង titrante ឬ Iodure ជាសូលុយស្យុង titrante
���. ក ខ និង គ
37. គេចង់ doser សារធាតុ X ដោយ Chromimétrie ។ គេចាក់សូលុយស្យុង Cr2O72- អោយលើសចូលទៅក្នុង សូលុយស្យុង X : X + Cr2O72- + 14 H+ 2 Cr3+ + 7 H2O + Y ។ បរិមាណ Cr2O72- ដែលលើសគេដាក់អោយមានប្រតិកម្មជាមួយ KI : Cr2O72- + 6 I- + 14H+ 2 Cr3+ + 7 H2O + 3 I2 ។ បន្ទាប់មក I2 ដែលកកើតត្រូវបានដាក់អោយមានប្រតិកម្មជាមួយ S2O32- : 2 S2O32- + I2 2 I- + S4O62- ។ បើគេដឹងថា ចំនួនម៉ូល Cr2O72- សរុបទាំងអស់ 1 moles ហើយ ចំនួនម៉ូល S2O32- ដែលគេប្រើស្មើនឹង 2,4 moles។ គណនាចំនួនម៉ូល X .
���. 0,6 moles
���. ០,4 moles
���. 1 moles
���. 2,4 moles
38. គេចាក់សូលុយស្យុង KI អោយលើសចូលទៅក្នុង សូលុយស្យុង hypochorite de sodium (NaClO) : ClO- + 2 I- + 2 H+ Cl- + I2 +H2O ។ L’iode ដែលកកើតត្រូវបាន dosé ដោយសូលុយស្យុង Thiosulfate de Na (Na2S2O3) : 2 S2O32- + I2 2 I- + S4O62- ប្រសិនគេដឹងថាគេប្រើ S2O32- អស់ 0,4 moles ។ ចូររកចំនួនម៉ូល NaClO ។
ក. 0,3 moles
���. 0.4 moles
���. 0.2 moles
���. 0.05 moles
39. Empois d’amidon អាចអោយយើងមើលឃើញបម្រែពណ៌ ក្នុង méthode de dosage ណាមួយ?
���. Dosage par iode
���. Manganimétrie
���. Chromimétrie
���. Dosage par Fe2+
40.គេរំលាយអាស៊ីត sulfurique 19.6 g ក្នុងទឹក 1L។ ចូរគណនា normalité របស់វា។ (ម៉ាស់ម៉ូលអាស៊ីត sulfurique = 98 g/mol)
ក. 0,4 N
���. 0,2 N
���. 0,4 M
���. 0,1 N
41. pH នៃសូលុយស្យុងដែលផ្ទុក KNO3 256mg (ម៉ាស់ម៉ូល=101 g/mol) គឺ
���. pH=2,7
���. pH=3
���. pH=7
���. pH=4
42. ចូរសរសេរទំនាក់ទំនងរវាង Ka និង Kb នៃគូអាស៊ីត/បាសមួយ។
���. Ka x Kb = Ke
���. Ka + Kb = Ke
���. Ka/Kb =Ke
���. Ka – Kb= Ki
43. អ្វីជាប្រតិកម្មអាស៊ីតបាស?
���. ប្រតិកម្មបន្ទេរអេឡិចត្រុង
ខ. ប្រតិកម្មបន្ទេរប្រូតុង
គ. ប្រតិកម្មបន្ទេរកាបូន
���. ប្រតិកម្មជំនួស
���.គ្មានចម្លើយត្រឹមត្រូវ
44.ចូររៀបអាស៊ីតខាងក្រោមតាមកំលាំងអាស៊ីតពីខ្លាំងទៅខ្សោយ
- acide méthanoïque , pKa=3.8
- acide fluorhydrique, pKa=3.2
- acide éthanoïque, pKa=4.6
ក. Acide fluorhydrique > acide méthanoïque > acide éthanoïque
���. Acide méthanoïque > acide éthanoïque > acide fluorhydrique
���. Acide éthanoïque > acide fluorhydrique > acide méthanoïque
���. Acide éthanoïque > acide méthanoïque > acide fluorhydrique
45.ដើម្បីរក volume របស់ solution titrante ក្នុង titration acido-basique នៅចំនុចសមមូល គេប្រើវិធីអ្វីខ្លះ?
ក. ដោយប្រើ indicateur coloré (titration colorimétrique)
ខ. ដោយប្រើ courbe potentiométrique
���. ដោយប្រើ courbe de pH (titration pH-métrique)
���. ចម្លើយ ក និង គ
46. Indicateur coloré ឈ្មោះអ្វីដែលគេប្រើក្នុងពេល dosage acide fort ដោយ NaOH រឺ dosage base forte ដោយ HCl ?
���. Hélianthine
���. Bleu de bromothymol
���. Phénophtaléine
���. Empois d’amidon
47. Indicateur coloré ឈ្មោះអ្វីដែលគេប្រើក្នុងពេល dosage acide faible ដោយ NaOH ?
���. Hélianthine
���. Bleu de bromothymol
���. Phénophtaléine
���. Empois d’amidon
48. Indicateur coloré ឈ្មោះអ្វីដែលគេប្រើក្នុងពេល dosage base faible ដោយ HCl ?
���. Hélianthine
���. Bleu de bromothymol
���. Phénophtaléine
���. Empois d’amidon
49. ដើម្បីរក volume របស់ solution titrante ក្នុង titration par oxydo-réduction នៅចំនុចសមមូល គេប្រើវិធីអ្វីខ្លះ?
���. ដោយប្រើ indicateur coloré (titration colorimétrique)
���. ដោយប្រើ courbe potentiométrique
���. ដោយប្រើ courbe de pH (titration pH-métrique)
���. ចម្លើយ ក និង ខ
���. ចម្លើយ ក ន៨ងគ
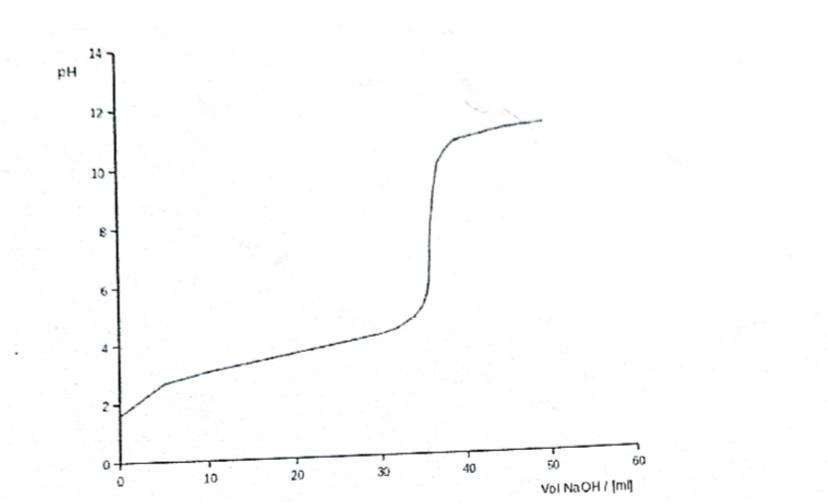
���. 45 mL
���. 20 mL
���. 30 mL
���. 35 mL
{"name":"Chimie analytique-Moeung Sotheara", "url":"https://www.quiz-maker.com/QPREVIEW","txt":"1. គេមានសូលុយស្យុងមួយដែលមានផ្ទុកសារធាតុ x ។ ចូរជ្រើសរើសចម្លើយដែលត្រឹមត្រូវ :, 2. គេមានសូលុយស្យុងមួយដែលមានផ្ទុកសារធាតុ x ។ ចូរជ្រើសរើសចម្លើយដែលត្រឹមត្រូវ :, 3. ខាងក្រោមនេះណាមួយជាទំនាក់ទំនងរវាង pH និង pKa របស់អាស៊ីតខ្សោយ :","img":"https://www.quiz-maker.com/3012/images/ogquiz.png"}
More Quizzes
Hope quiz
20100
Warframe quizz
10512
Duck Confit
100
Tema 1 CFU
301534
Percy Jackson Alexis Knapp: Prove You're a True Fan
201029697
Endocrine System: Test Your Hormone & Gland Knowledge
201027865
Should I Get a Tattoo? Take Our Tattoo Readiness
201030031
All of the Following Are Ionic Compounds Except?
201039971
Free Scatter Plot, Line of Best Fit Exam Answers
201023152
Which Celebrity Are You? Discover Your Star Personality
201023152
Master the Teacher Assistant Test: Free Practice
201050236
Am I Obsessed? Find Out If You're Crushing Too Hard
201026286