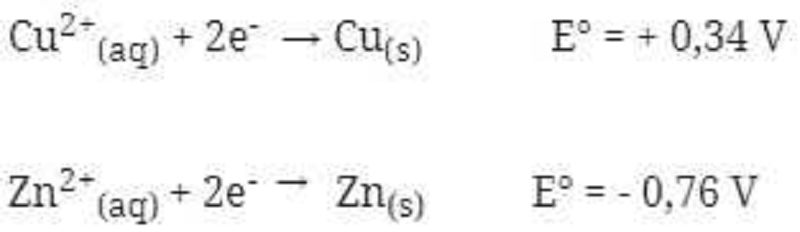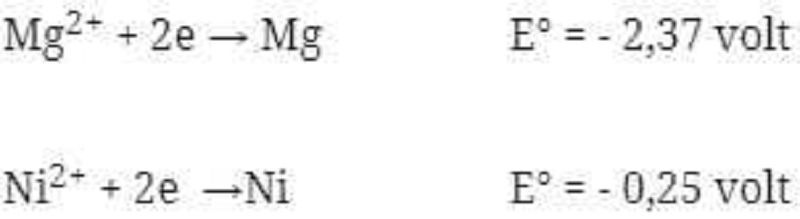SEL VOLTA
{"name":"SEL VOLTA", "url":"https://www.quiz-maker.com/QPREVIEW","txt":"Test your knowledge on electrochemical cells with our engaging quiz! Dive into the fascinating world of voltaic and electrolytic processes, understand the principles of oxidation and reduction, and explore the materials involved in electrochemical reactions.This quiz is perfect for students and enthusiasts of chemistry and electrochemistry.Multiple choice questionsCovers key concepts of electrochemistryFun and educational!","img":"https:/images/course2.png"}